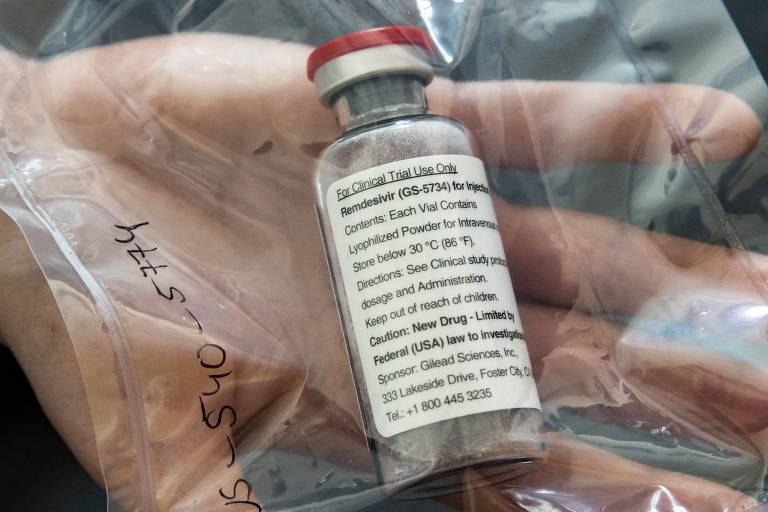
Indústria afirma que licença compulsória pode levar Brasil a ser preterido na venda de vacinas
by Patrícia Campos Mello | Folha de São PauloA indústria farmacêutica acusa o projeto de lei de licenciamento compulsório de remédios e vacinas contra covid-19, que deve ser votado na quinta-feira (29) no Senado, de ser um ato de “oportunismo”, e diz que a quebra de patentes pode levar os laboratórios a preterirem o Brasil na hora de fornecer medicamentos.
“É um movimento oportunista, muito bem orquestrado, que se aproveita da covid-19 para tentar quebrar patente”, diz Elizabeth de Carvalhaes, presidente executiva da Interfarma (Associação da Indústria Farmacêutica de Pesquisa), que representa 51 laboratórios, entre eles a Pfizer, Gilead e AstraZeneca.
Segundo Carvalhaes, se o Brasil fizer licenciamento compulsório, grandes laboratórios como Janssen, Pfizer e AstraZeneca podem preferir fornecer para outros mercados. “Não é retaliação. A demanda é muito maior que a oferta, e eles podem achar mais vantajoso, do ponto de vista econômico, vender para países que não quebram patente”, diz Carvalhaes.
O substitutivo do projeto de lei, relatado pelo senador Nelsinho Trad (PSD-MS), permite que o governo imponha licenciamento compulsório de remédios e vacinas (fabricação sem autorização prévia do detentor da patente) em caso de emergência nacional ou interesse público. Isso já estava previsto na lei de propriedade industrial atualmente em vigor, a 9.279 de 1996.
Mas o projeto, segundo Trad, dá agilidade, pois estabelece que o Ministério da Saúde deverá publicar, em até 30 dias após a a entrada em vigor da lei ou a decretação de emergência de saúde pública, uma lista de patentes cujas licenças compulsórias seriam necessárias.
O projeto também prevê negociação entre farmacêuticas e governos: se o Executivo considerar que os laboratórios assumiram compromissos objetivos de licenciamento voluntário (como por exemplo o acordo entre a AstraZeneca e a Fiocruz para transferência de tecnologia da vacina) ou de redução de preço de venda, não é feito o licenciamento compulsório.
O texto é bem mais palatável às farmacêuticas do que o projeto original, de autoria do senador Paulo Paim (PT-RS), que previa suspensão automática de todas as patentes de medicamentos, testes e vacinas relacionados à covid.
“Vivemos um problema sanitário sem precedentes, mas quebrar patentes não vai aumentar o acesso a vacinas e remédios”, diz Carvalhaes. “Não existem remédios contra covid-19, apenas medicamentos acessórios, e a maioria são remédios antigos.”
De fato, dexametasona e anticoagulantes, usados em pacientes hospitalizados, e anestésicos e neurobloqueadores, necerssários para intubação, são remédios antigos, cujas patentes expiraram, na maioria dos casos.
Mas não é o caso do remdesivir (Gilead) e da terapia de anticorpos monoclonais REGEN-CoV2, com casirivimabe e imdevimabe (Regeneron e Roche), que foram aprovadas pela Anvisa para uso em pacientes com covid. Alguns estudos apontam redução do tempo de internação com o remdesivir, embora a Organização Mundial de Saúde (OMS) não o recomende, e a Agência de Alimentos e Drogas (FDA) americana indica o Regen-CoV2 como eficaz para ajudar a evitar a hospitalização.
Nos EUA, o tratamento com remdesivir sai por US$ 520 (R$ 2860) a ampola, ou cerca de US$ 3120 (R$ 17,1 mil) o tratamento. A farmacêutica ainda não anunciou o preço para o Brasil.
Farmacêuticas de Bangladesh estão fabricando a versão genérica do remdesivir e vendendo por US$ 65 (R$ 357) a ampola, ou US$ 390 (R$ 2.145) o tratamento todo. A Gilead não concedeu licença para farmacêuticas de Bangladesh produzirem o remédio, como fez com empresas da Índia, Paquistão e Egito. Mas as empresas de Bangladesh conseguiram fabricar o remdesivir fazendo engenharia reversa, e estão exportando para 21 países, entre eles Filipinas, Venezuela e Líbano.
Bangladesh, por ser parte do grupo das nações menos desenvolvidas (LDC), é autorizado, pelo acordo Trips da OMC, a fabricar remédios patenteados sem autorização dos donos das patentes e exportar para países que também estejam entre os LDC ou tenham licença compulsória do medicamento.
Com licenciamento compulsório no Brasil, o país poderia comprar genéricos do remdesivir de Bangladesh, por exemplo.
Isso vai contra um dos principais argumentos da indústria farmacêutica e do governo brasileiro – de que não adianta pedir licença compulsória do remédio, porque o Brasil vai demorar muito para conseguir replicar o medicamento. Com a licença compulsória, enquanto não replica, pode importar de países que fabricam genéricos.
Foi o que aconteceu no Brasil em 2007, quando o governo brasileiro decretou a licença compulsória do Efavirenz, um dos antirretrovirais do coquetel para tratamento do HIV.
O governo brasileiro tentou negociar com a detentora da patente, a Merck Sharp & Dohme, uma redução no preço – queria que o comprimido, vendido a US$ 1,59 no Brasil, fosse comercializado pelo mesmo preço praticado na Tailândia, de US$ 0,65. A farmacêutica ofereceu desconto bem menor, propôs vender a US$ 1,11 o comprimido. O governo brasileiro não aceitou, e decretou o licenciamento compulsório.
No início, o governo importou o genérico do Efavirenz de laboratórios na Índia, que repassaram a tecnologia para produção nacional pelo laboratório Farmanguinhos, da Fiocruz. O genérico já era cerca de 70% mais barato que o patenteado. Depois de dois anos, o Farmanguinhos começou a produzir o genérico do efavirenz, a um preço bem menor do que remédio patenteado era vendido no país, e pagando royalties à Merck Sharp & Dohme.
Mas o caso das vacinas é mais complicado. Nenhum país conseguiu, até agora, fazer engenharia reversa de vacinas para covid. No Brasil, o Butantã tem parceria com a Sinovac e a Fiocruz, com a AstraZeneca. Mesmo com acordo de transferência de tecnologia, os laboratórios ainda não estão efetivamente fabricando completamente as vacinas.
Opositores da lei afirmam que não é necessário ter nova legislação, uma vez que a atual lei de propriedade intelectual e o acordo Trips da OMC já permitem que os países baixem licenças compulsórias em casos de “emergência nacional”.
Mesmo assim, isso raramente é feito, por medo de retaliações dos laboratórios e dificuldade de replicar os medicamentos. No Brasil, ocorreu uma única vez, em 2007, com o Efavirenz.
“Essa lei pode criar insegurança no Brasil e criar dificuldades na OMC”, diz Nelson Mussolini, presidente da Sindusfarma (Sindicado da indústria de produtos farmacêuticos do estado de São Paulo). Além do mais, diz Mussolini, a patente não é o que está dificultando a compra de vacinas – o que falta é capacidade. “O Brasil vai conseguir começar a produzir amanhã essas vacinas?”, pergunta. “Essa é uma discussão populista que não vai gerar efeitos práticos para a população, e pode até dificultar a entrada do Brasil na OCDE.”
No fim do ano passado, Índia e África do Sul, com apoio de mais de 110 países em desenvolvimento, fizeram uma proposta na OMC para suspender todas as patentes relacionadas a medicamentos e vacinas de covid enquanto durar a pandemia. Dessa maneira, argumentaram, seria possível aumentar a produção em países pobres. Por enquanto, cerca de 90% das vacinas foram aplicadas em habitantes de países ricos ou de renda média.
Países como EUA, Reino Unido e União Europeia, onde foram desenvolvidas as vacinas, bloquearam a iniciativa da Índia. O Brasil se alinhou aos países ricos e ficou contra a proposta.
A indústria argumenta que a quebra de patentes retira os incentivos dos laboratórios de investir em pesquisa e desenvolvimento, cruciais para a descoberta de novas drogas. Especialistas concordam, mas apontam que, no caso de muitos medicamentos e vacinas para Covid, grande parte do investimento veio de governos, e, por isso, as empresas deveriam praticar preços menores e aumentar o fornecimento.
Neste mês, o Brasil anunciou apoio a uma espécie de terceira via na OMC. A proposta é identificar países onde há capacidade ociosa de produção e estimular as farmacêuticas a fazerem transferência de tecnologia, voluntariamente. A iniciativa teria financiamento de bancos de desenvolvimento como Banco Mundial e Bid.
Ativistas estão céticos. “Vimos o que aconteceu com o C-Tap (pool de acesso a tecnologia) lançado pela OMS no ano passado – foi um fiasco, os laboratórios não colaboraram”, diz Pedro Villardi, coordenador do Grupo de Trabalho em Propriedade Intelectual (GTPI). A ideia do C-TAP era fazer um pool de compartilhamento de tecnologias, dados e patentes relacionadas à covid, mas a iniciativa não avançou.
No caso do projeto de lei que deve ser votado na semana que vem, a ideia é também ser uma espécie de “terceira via”- uma legislação de licença compulsória que funcione como instrumento de pressão sobre as farmacêuticas. Em negociação, os laboratórios concordariam com transferência de tecnologia e redução de preços para evitar a licença compulsória.
Foi o que fez o então ministro da saúde José Serra com o Nelfinavir, um dos medicamentos do coquetel anti-HIV. Em 2001, Serra ameaçou fazer licença compulsória, e o laboratório acabou reduzindo em 40% o preço.
Mas críticos apontam fragilidades no projeto de lei. Vai depender do Ministério da Saúde elaborar uma lista de remédios e vacinas alvos de licença compulsória. Uma vez que o governo federal é abertamente contra o uso de licenciamento compulsório, o Ministério pode publicar uma lista sem nenhum medicamento, dizendo, por exemplo, que o Brasil não conseguiria fazer engenharia reversa.
Além disso, ativistas acham que as farmacêuticas podem fazer corpo mole. Não há prazo para a negociação entre as farmacêuticas e o Ministério da Saúde, e o órgão pode suspender o pedido de licença compulsória diante de meras “promessas” de transferência de tecnologia.
"A licença compulsória é essencial para alcançar tratamento e vacinação em massa, e, em tempos de emergência, deveria ser tornada a regra e não a exceção. Esperamos que o senado caminhe nessa direção, até mesmo porque já é amplamente verificado que as licenças voluntárias falharam e não podem continuar sendo a única opção. O substitutivo precisa fazer da licença compulsória uma política de Estado, que não esteja sujeita à posição do governo nem à pressões da indústria farmacêutica”, diz Villardi.
Procurado, o Ministério da Saúde afirmou: “A Anvisa acompanha a tramitação dos projetos de lei sobre licenciamento compulsório de medicamentos e vacinas no Congresso Nacional e se manifestará oportunamente.”
Comentários