A Anvisa esclarece que os dados pré-clínicos da CoronaVac não condizem com o que foi afirmado de que dados referentes à fase 3 já haviam sido entregues.
A Anvisa informou, nessa quinta-feira (26), que a vacina CoronaVac não terá aprovação automática no Brasil. A Agência Nacional de Vigilância Sanitária é responsável pelo controle sanitário no Brasil.
A agência informou ainda, por meio de nota, não ter recebido a maior parte da documentação necessária em relação à CoronaVac.
Isso significa, entretanto, que, uma eventual aprovação da vacina na China não terá liberação imediata aqui.
A China, por seu turno, é o país de origem dessa vacina, conforme publicação do R7.
De acordo com o órgão, no processo criado para facilitar o registro o Instituto Butantan forneceu poucos dados.
O processo criado, nesse sentido, é o chamado “submissão continuada”. O Butantan, portanto, é parceiro da fabricante Sinovac no Brasil.
O instituto forneceu apenas “dados pré-clínicos, que são dados anteriores aos testes com seres humanos”, informou a Anvisa.
Por outro lado, os dados pré-clínicos não condizem com o que foi afirmado de que dados referentes à fase 3 já haviam sido entregues.
Esforço desnecessário
A agência explica, no entanto, que tem “medidas para evitar retrabalho e esforços desnecessários” “E, por isso, é possível considerar análises realizadas por outras agências para sua decisão”.
Ressalta, contudo, “que o reconhecimento tácito da aprovação por outras agências para registro de vacinas aqui no Brasil não é previsto em lei”. Portanto, “pode representar risco à população brasileira”.
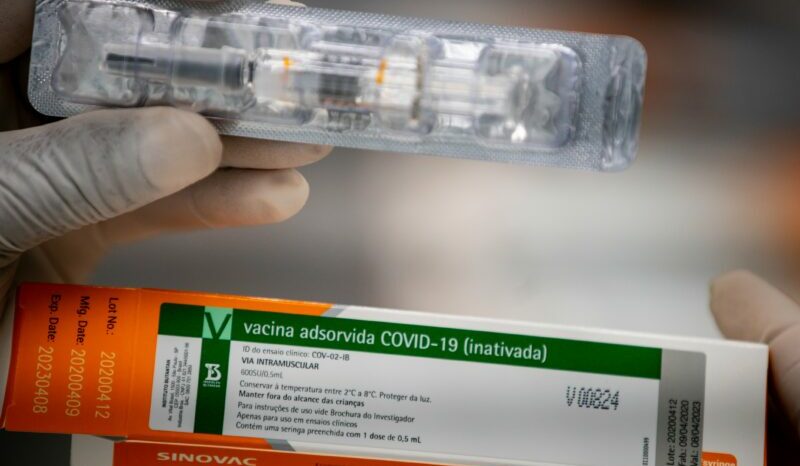
Foto: Instituto Butantan/divulgação
Comentários