SÃO PAULO — A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou na terça-feira (18) as regras para registro comercial no Brasil de terapias de saúde com modificação de DNA ou células cultivadas em laboratório. Técnicas deste tipo eram regulamentadas antes apenas para uso experimental.
O texto normativo aprovado pela diretoria colegiada da Anvisa classifica esses tratamentos como "terapias avançadas".
A agência diz que se enquadram na categoria qualquer técnica do gênero usada para "tratar, prevenir ou diagnosticar" doenças que não tenham cura ou tratamento por vias convencionais.
A área terapêutica inclui, por exemplo, o uso de células imunes geneticamente modificadas para combater o câncer, como foi feito com paciente recentemente em caráter experimental no Hospital de Clínicas de Ribeirão Preto.
Outro tipo de terapia enquadrado na nova normativa é o uso de vírus com DNA alterado para tentar modificar o material genético de pacientes com doenças hereditárias.
— Essa categoria é uma nova categoria de produto que tem prometido revolucionar a saúde no Brasil e no mundo — afirma em vídeo Renata Parca, especialista da Anvisa que participou da criação as novas regras. — Essa regulamentação trata dos critérios mínimos de qualidade, segurança e eficácia que têm de ser provados para que a Anvisa registre e aprove a comercialização desses produtos no país.
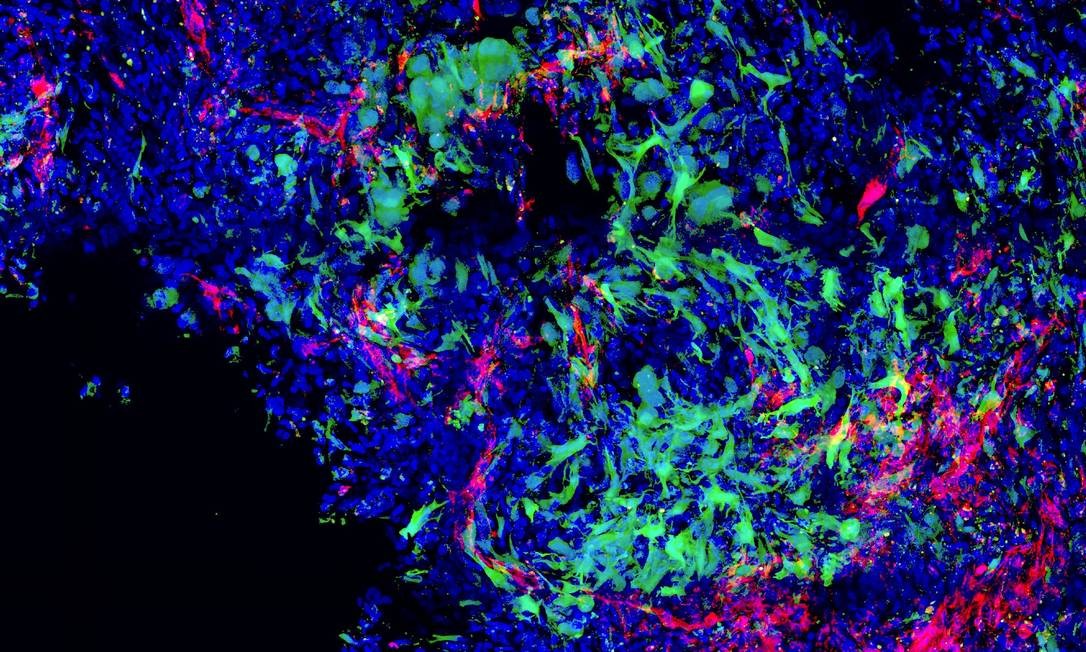 Imagem de microscópio mostra células tumorais (azul) atacadas por vírus geneticamente modificado para combater câncer de mama (verde) Foto: Sheena Smith / SNSF
Imagem de microscópio mostra células tumorais (azul) atacadas por vírus geneticamente modificado para combater câncer de mama (verde) Foto: Sheena Smith / SNSF
Comentários