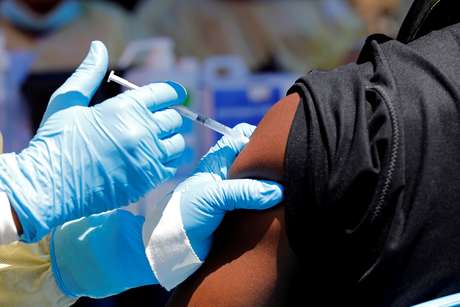
Agente de saúde aplica vacina para Ebola em morador de Goma, na República Democrática do Congo 05/10/2018 REUTERS/Baz Ratner - Foto: Reuters
A Johnson & Johnson disse que solicitou a aprovação da agência reguladora da Europa para sua vacina experimental de duas doses contra Ebola nesta quinta-feira, menos de um mês depois de a agência recomendar a liberação da vacina da Merck & Co.
A J&J disse ter apresentado à Agência Europeia de Remédios (EMA) dois pedidos de autorização de comercialização de seu regime de vacina destinado à cepa do vírus Ebola do Zaire, a que mais causa surtos da doença mortal.
A vacina da empresa exige duas injeções administradas com cerca de oito semanas de intervalo, a primeira desenvolvida com a tecnologia da J&J e a segunda fabricada pela companhia de biotecnologia dinamarquesa Bavarian Nordic A/S.
Os pedidos da Johnson & Johnson se amparam em dados de mais de 10 estudos que testaram o regime em adultos e crianças, informou a empresa.
A farmacêutica acrescentou que está debatendo com a Agência de Alimentos e Remédios dos Estados Unidos o conjunto de dados necessário para conseguir uma aprovação norte-americana.
Desde que começou, em agosto de 2018, o surto de Ebola já matou mais de duas mil pessoas, só ficando atrás da epidemia de 2013-2016 na África Ocidental, que matou mais de 11.300 pessoas.
A recomendação de aprovação da EMA para a vacina contra Ebola de dose única da Merck foi saudada pela Organização Mundial da Saúde (OMS) como um "triunfo para a saúde pública" que pode salvar muitas vidas.
Neste mês, autoridades de saúde da República Democrática do Congo estão adotando a vacina da Johnson & Johnson para combater o surto atual nas províncias do leste do país, onde a vacina da Merck já está sendo usada.
A Janssen, uma unidade da J&J, também está colaborando com a OMS para permitir o registro do regime de vacina contra Ebola em países africanos, disse a empresa.
Comentários